Chemilumineszenz
Luminol ist ein Reagenz, das Licht emittiert, wenn es mit Blut in Berührung kommt. Der erste Artikel, der die Verwendung als forensisches Werkzeug vorschlägt, wurde 1937 veröffentlicht [1] . Das Phänomen, dass Licht in einer chemischen Reaktion emittiert wird, nennt man Chemilumineszenz. Wenn ein Blutfleck mit Luminol besprüht wird, dauert die Chemilumineszenz etwa 10 Sekunden bis einige Minuten. Obwohl die Intensität des blau-weißen Lichts (Peak-Emission um 455 nm [7] ) ist nicht hoch, kann mit längeren Belichtungszeiten fotografiert werden. Durch erneutes Lackieren mit Luminol wird die Chemilumineszenz wieder sichtbar. Das Luminolreagens ist jedoch kein Fixiermittel und daher beginnt der Fleck langsam zu laufen. Vor allem nach mehreren Anwendungen.
Aus der obigen Beschreibung wird klar, dass eine erfolgreiche Suche nach Blut (und insbesondere das Fotografieren der Lumineszenz) nur in völliger Dunkelheit erfolgen kann. Entweder muss man nachts arbeiten oder man muss den Tatort verdunkeln.
Anwendungen
Luminol kann verwendet werden für:
- Auf der Suche nach Blut, wenn keine sichtbaren Spuren vorhanden sind. Aufgrund der Empfindlichkeit des Reagenz können Blutspuren, die gereinigt wurden, noch Lumineszenz zeigen. Beispiele sind der Einsatz in Häusern, Garagen und im Inneren von Autos.
- Aufzeichnen von Blutflecken wie Schuhabdrücke auf Teppichen, wo Farbstoffe wie Amido Black oder Hungararian Red ein totales Durcheinander verursachen würden. [2]
- Dokumentieren von Blutflecken auf Böden, Wänden und Decken (in diesem Fall zB von Messern).
- Suchen und Folgen von Blutspuren im Freien. In städtischen Gebieten ist dies oft schwierig zu realisieren, wegen der Straßenbeleuchtung und so weiter, es sei denn, man kann die Elektrizität im ganzen Gebiet abschalten. In Wäldern oder offenen Feldern ist dies weniger ein Problem. Es ist bekannt, dass Luminol von Jägern verwendet wird, um verwundete Tiere aufzuspüren.
Rezepte
Das Luminol-Set F-3000 (für 1 Liter Arbeitslösung) basiert auf einer bekannten und oft verwendeten Rezeptur (K. Weber, 1966). Das Set F-31000 (für 0,5 Liter Arbeitslösung) basiert auf einem konzentrierteren niederländischen Rezept, das auf der SPTM Konferenz in Stockholm [3] und das IAFS Konferenz in Los Angeles [4] im Jahr 1999 sowie in mehreren Artikeln in der niederländischen Zeitschrift diskutiert Modus [5] .
Das niederländische Rezept hat eine (konzentriertere) Zusammensetzung, die eine stärkere Chemilumineszenz als das klassische Weber-Rezept bietet. Obwohl es stärker ist, wird der (unvermeidliche) DNA-Abbau der Blutspuren auf ein akzeptables Niveau begrenzt.
Gebrauchsanweisung "Classic" Rezept F-30000
Dieses Set besteht aus drei Lösungen (alle auf Wasserbasis): eine Natriumhydroxidlösung (Lösung A), eine Lösung von Luminol (3-Aminophthalhydrazid / 5-Amino-2,3-dihydro-1,4-phthalazindion) in einer schwach basischen Lösung (Lösung C) und einer schwachen Wasserstoffperoxidlösung (Lösung B). Die Lösung B wird vom Benutzer hergestellt, indem zwei Tabletten eines Urea-Wasserstoffperoxid-Komplexes in dem (gelieferten) 100 ml destillierten Wasser gelöst werden. Das Mischungsverhältnis ist 1 Teil Lösung A, 1 Teil Lösung B und 1 Teil Lösung C verdünnt mit 7 Teilen Wasser (demineralisiertes oder destilliertes Wasser, nicht im Lieferumfang enthalten).
Nach der Vorbereitung der Arbeitslösung kann sie für mehrere Stunden verwendet werden (bei Raumtemperatur gilt, je niedriger die Temperatur, desto länger hält die Lösung). In Kontakt mit Blut, das als Katalysator wirkt, reagiert das Luminol mit Wasserstoffperoxid und setzt ein Molekül Stickstoff und (manchmal) Licht frei. Das Endprodukt ist 3-Aminophthalsäure (genauer gesagt Natriumsalze davon wegen der basischen Lösung). Je niedriger die Temperatur ist, desto geringer ist die Lumineszenz.
Die Arbeitslösung muss mit einem sehr feinen Nebel über die zu untersuchende Fläche gesprüht werden. Da sich ein Teil des Blutes in den Tröpfchen auflöst und dadurch die Spur diffundiert, ergeben feine Tröpfchen (Nebel) das beste Ergebnis.
Die besten Ergebnisse werden mit Sprühgeräten erzielt, die in Autoreparaturen und / oder Luftbürsten verwendet werden. Eine Abdruckluftquelle am Tatort ist dann eine Voraussetzung. Für alle Sprühgeräte ist es am besten, dass sie keine oder so wenig wie möglich Metallteile enthalten, da Metalle und Metalloxide auch die Reaktion zwischen Luminol und Wasserstoffperoxid katalysieren können.
Gebrauchsanweisung starke Rezept F-31000
Dieser Satz enthält eine Lösung (enthält Luminol und Natriumhydroxid in Wasser) und zwei Tabletten Urea-Wasserstoffperoxid-Komplex. Die Zugabe der zwei Tabletten zu der Lösung (oder einer Tablette zu der Hälfte der Lösung) und das Auflösen derselben ergibt die Arbeitslösung (0,5 Liter).
Aufgrund der höheren Konzentrationen der Chemikalien in diesem Rezept ist das Besprühen der Lösung in einem feinen Nebel noch wichtiger als bei der klassischen Rezeptur.
Fehlalarm
Es ist nicht nur Blut, das die Reaktion zwischen Luminol und Wasserstoffperoxid katalysiert. Bestimmte Pflanzenenzyme (gebrochene Stängel, zertrampeltes Gras, beschädigte Früchte), Materialien (wie Jute, Sisal, Rost, Kupferoxid, bestimmte Farben) [6] ), ebenso wie Oxidationsmittel wie Haushaltsbleiche.
Falsche positive Reaktionen können manchmal von denen des Bluts wegen eines geringen Farbunterschieds und / oder einer kürzeren Dauer der Lumineszenz unterschieden werden. Der Farbunterschied kann mit Spektrometern gesehen werden, ist jedoch mit bloßem Auge schwer oder gar nicht zu erkennen.
Interferenz der häufigsten falsch positiven, Bleichmittel, kann verhindert werden. Das in Bleichmitteln gefundene Hypochlorit zersetzt sich nach dem Trocknen in ein bis mehreren Tagen [10] . Wenn Bleichmittelkontamination vermutet wird, ist die beste Option, einen Tag oder länger vor der Untersuchung mit Luminol zu warten. Eine andere Möglichkeit ist die Verwendung der Grodsky-Luminolformulierung (Luminol, Natriumcarbonat, Natriumperborat in Wasser) [11] ) mit 0,1 mol / L 1,2-Diaminoethan (6 gram / Liter) [10] . Das 1,2-Diaminoethan reagiert schneller mit dem restlichen Bleichmittel als die Reaktion von Luminol mit Bleichmittel. Es verringert auch die Intensität und Dauer der Lumineszenz etwas.
Um zu vermeiden, dass falsch positive Bereiche für DNA abgetastet werden, kann der verdächtige Farbstoff mit anderen indikativen Tests auf Blut getestet werden. Das niederländische forensische Institut NFI empfiehlt den Tetra-Basistest [8] .
Fluorescein und Luminol
Mischen einer kleinen Menge Fluorescein oder reduziertem Fluorescein mit der Luminol-Arbeitslösung ergibt eine grüne Fluoreszenz (Peak-Emission um 520 nm) anstelle einer blau-weißen und wird berichtet, dass sie tatsächlich stärker ist als die von Luminol alleine. Mit Rhodamin-B wird eine violette Farbe erhalten (siehe auch youtube.com für Vorführungen in Flaschen oder Bechern).
Eine Reihe von wissenschaftlichen Artikeln zu diesem Phänomen finden Sie in den Referenzen 12.
Aufnahme (Fotografie und Video)
Die Lumineszenz von Luminol kann photographisch aufgezeichnet werden, obwohl eine große Linsenöffnung und lange Belichtungszeiten notwendig sind. Auch mehrere Spritzungen (eventuell mit gleichzeitiger Blutfleckung) können sich als notwendig erweisen.
Videoaufnahme ist möglich, benötigt aber einen Bildverstärker [3, 5b, 9] um nützlich zu sein.
Fußnoten und Referenzen
[1] Luminol wurde zum ersten Mal als forensisches Instrument zur Detektion von Blutspuren vorgeschlagen durch:
Sprecht, W., "Die Chemilumineszenz des Hämins, ein Hilfsmittel zur Auffindung und Erkennung forensisch wichtiger Blutspuren", Angew. Chem. 1937 Vol. 50, blz. 155-157.
Die Reaktion, die Licht liefern soll, ist die Zersetzung von oxidiertem Luminol zu 3-Aminophthalsäure und Stickstoff.
[2] Für diese Anwendung kann auch reduziertes Fluorescein ("Leuco" Fluorescein) verwendet werden. Dieses Reagenz nutzt die durch Blut induzierte Oxidation von reduziertem Fluorescein (nicht fluoreszierend) zu hoch fluoreszierenden Fluorescein. Die Fluoreszenz wird mit blauem Licht induziert und durch einen Gelbfilter betrachtet und fotografiert. Siehe zum Beispiel den Artikel auf Niederländisch von Renaat Develtere, Laboratoriumskommissar bei der Gerechtenijke Politie, Kortrijk, Belgien:
Develtere, R., "Fluoresceine, deteciemiddel voor latente bloedsporen", Modus , 2000 , Band 9, Nr. 4, p. 37-39 und die Referenzen in diesem Artikel.
PVC-Bodenbelag mit Schaumstoff im Blut 
Nach Behandlung mit reduziertem Fluorescein.

Beachten Sie, dass der Sprühnebel nicht fein genug war (nicht fluoreszierende Tröpfchen sichtbar über dem Schuhabdruck).
Fotografie: Polilight 500 bei voller Leistung (Abstand Lichtleiter etwa 1 Meter zu drucken) mit Downtoned 450 nm Licht, Gelbfilter, Belichtungszeit ca. 2 Sekunden.
[4] Eikelenboom, R .; Kloosterman, A. "Luminol revisited"; Vortrag auf der IAFS-Konferenz August 1999. Für eine Zusammenfassung siehe auch: Informationsbulletin für Schuhprint / Toolmark Examiners 2000 Vol. 6, Nr. 2, p. 24-25 (Veröffentlichung der Marken Arbeitsgruppe des ENFSI ).
[5a] Eikelenboom, R .; Kloosterman, A., "Luminol herbelicht", Modus , 1999 , Jaargang 8, Nr. 4, p. 23-27.
[5b] Eversdijk, M .; Gelderman, R., "Nieuw Licht op plaats Delikt", Modus , 1999 Vol. 8, Nr. 4, p. 28-30.
[6] Quicken, TI; Creamer, JI, "Eine Studie über häufige Interferenzen mit dem forensischen Luminol-Test für Blut" Lumineszenz , 2001 Vol. 16, Nr. 4, p. 295-298. DOI: 0.1002 / bio.657
[7] Quicken, TI; Cooper, PD, "Erhöhung der Spezifität des forensischen Luminol-Tests für Blut" Lumineszenz , 2001 Vol. 16, Nr. 3, p. 251-253. DOI: 10.1002 / bio.635
[8] Der Tetra-Basistest verwendet zwei Lösungen, die nur 1 Monat nach der Herstellung verwendet werden sollten: 0,5 g Tetra-Base (N, N, N ', N'-Tetramethyl-4,4'-diamino-diphenylmethan; CAS-Nr. [101-61-1]) in 100 ml 10% Essigsäure / Wasser und 5 g Bariumperoxid (BaO 2 ) in 100 ml 10% iger Essigsäure in Wasser. Lösen Sie sowohl die Tetra-Base als auch das Bariumperoxid in 10 ml konzentrierter Essigsäure vor dem Verdünnen mit 90 ml destilliertem Wasser, um die jeweiligen Lösungen davon herzustellen.
Falten Sie ein Stück rundes Filterpapier zweimal und reiben Sie mit der Spitze über den Bereich, der vermutlich getrocknetes Blut enthält. Dann sollten Sie den Filter aufklappen und einen Tropfen Tetrabaselösung zugeben. Nach Zugabe eines Tropfens der Bariumperoxidlösung sollte im Falle von Blut eine sofortige Blaufärbung sichtbar sein.
WARNUNG: Tetra-Base ist als wahrscheinlich krebserzeugend für den Menschen eingestuft. Daher sollte die Arbeitslösung in einem Abzug hergestellt und Maßnahmen ergriffen werden, um den Kontakt mit dem Stoff zu vermeiden.
[9] Shirk, SA, "Night Vision Video und Luminol", Journal für forensische Identifizierung , 1995 Vol. 45, Nr. 5, 513-514.
[10] Kent, EJM; Douglas, AE; Miskelly, GM, "Hemmung der bleichinduzierten Luminol-Chemilumineszenz", Zeitschrift für Forensische Wissenschaften , 2003 Vol. 48, Nr. 1, p. 66-67. DOI: 10.1520 / JFS2002105
[11] Grodsky Rezept für Luminol: 1 g Luminol, 50 g Na 2 CO 3 , 7 g NaBO 3 .4H 2 O (Natriumperborat) in 1 l destilliertem Wasser. Grodsky, M., Wright, K., Kirk, PL "Vereinfachte vorläufige Bluttests. Eine verbesserte Technik und eine vergleichende Methodenlehre. ", Das Journal für Strafrecht, Kriminologie und Polizeiwissenschaft , 1951 Vol. 42, Nr. 1, S. 95-104. DOI: 10.2307 / 1140307
[12a] Kalkar, CD; Doshi, SV; Madhuri Pendse, "Aqualumineszenz von alkalischem Luminol in Gegenwart von Fluorescein" Internationale Zeitschrift für Strahlenanwendungen und Instrumentierung. Teil A. Angewandte Strahlung und Isotope , 1986 Vol. 37, Nr. 1, p. 41-45. DOI: 10.1016 / 0883-2889 (86) 90194-2
[12b] Navas Díaz, A; González García, JA; Lovillo, J. "Enhancer-Effekt von Fluorescein auf die Luminol-H2O2-Meerrettich-Peroxidase-Chemilumineszenz: Energietransferprozess.", J. Biolumin. Chemilumin. , 1997 Vol. 12, Nr. 4, p. 199-205. DOI: 10.1002 / (SICI) 1099-1271 (199707/08) 12: 4 <199::AID-BIO445> 3.0.CO; 2-U
[12c] Voicescu, M., Vasilescu, M., Meghea, A., "Energietransfer vom Aminophthalat Dianion zu Fluorescein", Journal der Fluoreszenz , 2000 Vol. 10, Nr. 3, p. 229-229. DOI: 10.1023 / A: 1009420320833
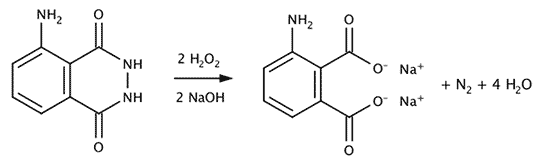
Zersetzung von Luminol durch Wasserstoffperoxid und Blut als Katalysator.
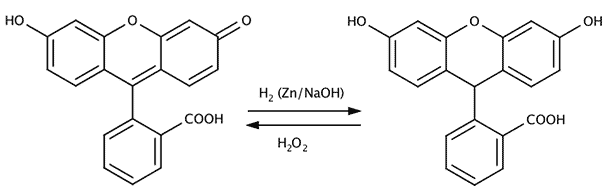
Fluorescein (fluoresziert unter blauem Licht) links, reduziertes Fluorescein (fluoresziert nicht) auf der rechten Seite.